Chuyên đề Cấu trúc phân tử hợp chất hữu cơ
I. LÍ THUYẾT TRỌNG TÂM
1. Công thức cấu tạo
|
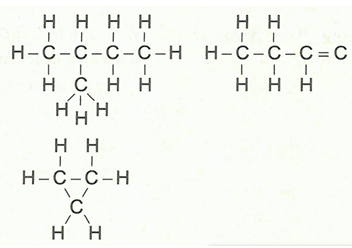
Định nghĩa: Công thức cấu tạo biểu diễn thứ tự và cách thức liên kết của các nguyên tử trong phân tử. Các loại công thức cấu tạo: Có cách viết khai triển, thu gọn và thu gọn nhất. CTCT KHAI TRIỂN
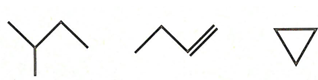
CTCT THU GỌN
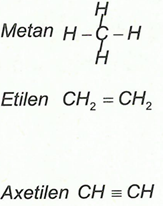
CTCT THU GỌN NHẤT 2. Thuyết cấu tạo hóa học a. Trong phân tử hợp chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hoá trị và theo một thứ tự nhất định – cấu tạo hóa học.
b. Trong phân tử hợp chất hữu cơ, cacbon có hoá trị IV. Nguyên tử cacbon có thể liên kết với nhau thành mạch cacbon. c. Tính chất của các chất phụ thuộc vào thành phần phân tử (bản chất, số lượng các nguyên tử) và cấu tạo hoá học (thứ tự liên kết các nguyên tử).
* Ý nghĩa: Thuyết cấu tạo hóa học giúp giải thích được hiện tượng đồng đẳng, hiện tượng đồng phân. 3. Đồng đẳng, đồng phân a. Khái niệm đồng đẳng Những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hóa học tương tự nhau là những chất đồng đẳng, chúng hợp thành dãy đồng đẳng.
b. Khái niệm đồng phân Những hợp chất khác nhau nhưng có cùng công thức phân tử được gọi là các chất đồng phân của nhau. Các loại đồng phân cấu tạo: Đồng phân mạch cacbon. Đồng phân vị trí liên kết bội. Đồng phân loại nhóm chức. Đồng phân vị trí nhóm chức. 4. Liên kết hóa học và cấu trúc phân tử hợp chất hữu cơ Liên kết hóa học thường gặp nhất trong phân tử các hợp chất hữu cơ là liên kết cộng hóa trị.
|
Chú ý: Công thức cấu tạo khai triển: Viết tất cả các nguyên tử và các liên kết giữa chúng.
Công thức cấu tạo thu gọn: Viết gộp nguyên tử cacbon và các nguyên tử khác liên kết với nó thành từng nhóm.
Công thức cấu tạo thu gọn nhất: Chỉ viết các liên kết và nhóm chức, đầu mút của các liên kết chính là các nhóm CHx với x đảm bảo hoá trị 4 ở C.
Ví dụ: Công thức phân tử C2H6O có hai công thức cấu tạo: : Đimetyl ete, chất khí, không tác dụng với Na. : Ancol etylic, chất lỏng, tác dụng với Na giải phóng hiđro.
Ví dụ: Phụ thuộc thành phần phân tử: CH4 là chất khí dễ cháy, CCl4 là chất lỏng không cháy. Phụ thuộc cấu tạo hoá học: CH3CH2OH và CH3OCH3 khác nhau cả về tính chất vật lí và tính chất hoá học.
Ví dụ: Các hiđrocacbon: CH2, C2H6, C3H8, C4H10, C5H12,…., CnH2n+2 Các cancol: CH3OH, C2H5OH, C3H7OH, C4H9OH,… CnH2+1OH
Ví dụ: Etanol (C2H5OH) và đimetyl ete (CH3OCH3) là hai chất khác nhau (có tính chất khác nhau) nhưng lại có cùng công thức phân tử là C2H6O.
|
II. CÁC DẠNG BÀI TẬP
Dạng 1: Hiện tượng đồng đẳng
Phương pháp giải
|
Dựa vào khái niệm đồng đẳng để đánh giá các chất có thuộc cùng dãy đồng đẳng hay không.
Nhận diện được những điểm tương tự nhau trong các công thức cấu tạo cho trước. Lập được công thức chung của các dãy đồng đẳng theo dữ kiện cho trước với công thức tính độ bất bão hòa trong phân tử: số + số vòng đơn. Trong đó: k: độ bất bão hòa của phân tử. số nguyên tử C, H, O trong phân tử. |
Ví dụ: Cho các chất sau đây:
Các chất đồng đẳng của nhau là A. I, II và VI. B. I, III và IV. C. II, III, V và VI. D. I, II, III và IV. Hướng dẫn giải Xét các chất có cùng Loại B, D. Xét tiếp các chất có nhóm OH gắn với các nguyên tử C bậc I: (II), (III), (V), (VI). Các chất thuộc dãy đồng đẳng ancol no, đơn chức, bậc I. Chọn C. |
Ví dụ mẫu
Ví dụ 1: Trong các dãy chất sau đây, dãy nào gồm các chất là đồng đẳng của nhau?
A. B.
C. D.
Hướng dẫn giải
Xét các chất có thành phần hơn kém nhau một hay nhiều nhóm CH2.
Xét các chất có đặc điểm cấu tạo tương tự nhau.
Chọn A.
Ví dụ 2: Công thức chung của dãy đồng đẳng hiđrocacbon mạch hở chứa một nối đôi và một nối ba trong phân tử là
A. B.
C. D.
Hướng dẫn giải
Xuất phát từ công thức chung của hiđrocacbon mạch hở với k là số liên kết trong phân tử.
Hiđrocacbon có một nối đôi và một nối ba Tổng số liên kết
Công thức chung cần tìm là
Chọn B.
III. Bài tập tự luyện dạng 1
Bài tập cơ bản
Câu 1: Định nghĩa đồng đẳng nào sau đây là đúng?
A. Những chất đồng đẳng là những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hóa học tương tự nhau.
B. Những chất đồng đẳng là những đơn chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hóa học tương tự nhau.
C. Những chất đồng đẳng là những hợp chất có thành phần phân tử hơn kém nhau một nhóm CH2 nhưng có tính chất hóa học tương tự nhau.
D. Những chất đồng đẳng là những hợp chất có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hóa học khác nhau.
Câu 2: Công thức C6H6 thuộc dãy đồng đẳng nào sau đây?
A. B.
C. D.
Câu 3: Các chất nào sau đây thuộc dãy đồng đẳng có công thức chung ?
A.
B.
C.
D.
Câu 4: Chất nào sau đây là đồng đẳng của benzen?
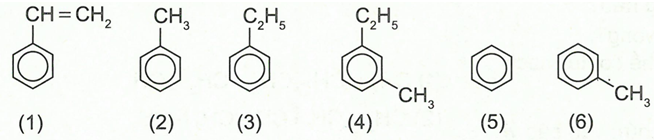
A. B.
C. D.
Câu 5: Vitamin A công thức phân tử C20H30O, có chứa một vòng sáu cạnh và không có chứa liên kết ba. Số liên kết đôi trong phân tử vitamin A là
A. 7. B. 6.
C. 5. D. 4.
Câu 6: Cho các chất: C6H5OH (X); C6H5CH2OH (Y); HOC6H4OH (Z); C6H5CH2CH2OH (T). Các chất đồng đẳng của nhau là:
A. Y, T. B. X, Z, T.
C. X, Z. D. Y, Z.
Câu 7: Công thức tổng quát của dẫn xuất điclo mạch hở có chứa một liên kết ba trong phân tử là
A. B.
C. D.
Câu 8: Licopen, công thức phân tử C40H56 là chất màu đỏ trong quả cà chua, chỉ chứa liên kết đôi và liên kết đơn trong phân tử. Hiđro hóa hoàn toàn licopen được hiđrocacbon C40H82. Licopen có:
A. 1 vòng; 12 nối đôi. B. 1 vòng; 5 nối đôi.
C. 4 vòng; 5 nối đôi. D. mạch hở; 13 nối đôi.
Câu 9: Metol C10H20O và menton C10H18O chúng đều có trong tinh dầu bạc hà. Biết phân tử metol không có nối đôi, còn phân tử menton có 1 nối đôi. Phát biểu nào sau đây đúng?
A. Metol và menton đều có cấu tạo vòng.
B. Metol có cấu tạo vòng, menton có cấu tạo mạch hở.
C. Metol và menton đều có cấu tạo mạch hở.
D. Metol có cấu tạo mạch hở, menton có cấu tạo vòng.
Bài tập nâng cao
Câu 10: Ba hiđrocacbon X, Y, Z là đồng đẳng kế tiếp, khối lượng phân tử của Z bằng 2 lần khối lượng phân tử của X. Đốt cháy 0,1 mol chất Y, sản phẩm khí hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư, thu được khối lượng kết tủa là
A. 20 gam. B. 40 gam.
C. 30 gam. D. 10 gam.
Dạng 2. Hiện tượng đồng phân
Phương pháp giải
|
Công thức phân tử hợp chất hữu cơ có dạng:
Bước 1: Tính độ bất bão hòa k của phân tử.
= số liên kết + số vòng đơn. Với k = 0 Hợp chất chỉ có liên kết đơn. Với k = 1 Hợp chất có một liên kết đôi hoặc có một vòng đơn. Bước 2: Xác định các đồng phân cần viết theo yêu cầu của bài tập. Hợp chất thuộc dãy đồng đẳng nào? Hợp chất mạch hở hay mạch vòng? Bước 3: Viết khung mạch cacbon có thể có, từ mạch dài nhất đến mạch ngắn nhất. Bước 4: Thêm nối đôi, nối ba, nhóm chức vào các vị trí thích hợp trên mạch cacbon. Điền số nguyên tử H để cacbon đủ hóa trị IV.
Chú ý: Nếu đề bài hỏi số đồng phân thì tính cả đồng phân hình học còn đề bài hỏi số đồng phân cấu tạo thì không tính đồng phân hình học: Điều kiện cần: Có liên kết đôi hoặc vòng.
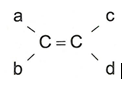
Điều kiện đủ: Hai dạng đồng phân hình học:
|
Ví dụ: Số đồng phân cấu tạo ứng mạch hở ứng với công thức phân tử C5H10 là A. 6. B. 2. C. 3. D. 5. Hướng dẫn giải Độ bất bão hòa:
Vì k = 1, mạch hở Phân tử có một liên đôi C = C. Có đồng phân về mạch C và vị trí nối đôi.
Có 5 đồng phân cấu tạo thỏa mãn. Chọn D. Ví dụ: Số đồng phân ứng mạch hở ứng với công thức phân tử C5H10 là A. 6. B. 2. C. 3. D. 5. Hướng dẫn giải Tương tự ví dụ trên nhưng tính cả đồng phân hình học. Đồng phân số (2) có đồng phân hình học (cis, trans) nên tổng số đồng phân là 6. Chọn A. |
Ví dụ mẫu
Ví dụ 1: ứng với công thức phân tử C4H10O có bao nhiêu cấu tạo khác nhau chứa nhóm OH?
A. 2. B. 3.
C. 4. D. 5.
Hướng dẫn giải
Độ bất bão hòa: Phân tử chỉ có liên kết đơn.
Có bốn công thức thỏa mãn là:
Chọn C.
IV. Bài tập tự luyện dạng 2
Bài tập cơ bản
Câu 1: Đồng phân là
A. những hợp chất khác nhau nhưng có cùng công thức phân tử.
B. những đơn chất khác nhau nhưng có cùng công thức phân tử.
C. những hợp chất giống nhau và có cùng công thức phân tử.
D. những hợp chất khác nhau nhưng có cùng dạng công thức cấu tạo.
Câu 2: Cặp chất nào sau đây là đồng phân của nhau?
A. và
B. và
C. và
D. và
Câu 3: Số đồng phân của hợp chất có công thức phân tử là
A. 2. B. 3.
C. 4. D. 5.
Câu 4: Hợp chất X có công thức phân tử là C3H6. Số đồng phân của X là
A. 1. B. 2.
C. 3. D. 4.
Câu 5: Số đồng phân ứng với công thức phân tử C3H5Cl là
A. 3. B. 4.
C. 5. D. 6.
Câu 6: Số đồng phân mạch hở ứng với công thức phân tử C3H6O là
A. 2. B. 3.
C. 4. D. 5.
Câu 7: Những công thức cấu tạo nào sau đây biểu diễn cùng một chất?
A. B.
C. D.
Câu 8: Cho các chất sau: và . Chất có nhiều đồng phân cấu tạo nhất là
A. B. .
C. . D. .
Câu 9: Cho các chất: và Chất có nhiều đồng phân cấu tạo nhất là
A. . B. .
C. . D.
Bài tập nâng cao
Câu 10: Đốt cháy hoàn toàn V lít khí của mỗi hiđrocacbon X, Y, Z đều thu được 4V lít CO2 và 4V lít H2O. Phát biểu nào sau đây là đúng?
A. Ba chất X, Y, Z là các đồng phân của nhau.
B. Ba chất X, Y, Z là các đồng đẳng của nhau.
C. Ba chất X, Y, Z là đồng phân hình học của nhau.
D. Ba chất X, Y, Z là đồng phân cấu tạo của nhau.
PHẦN ĐÁP ÁN
Dạng 1: Hiện tượng đồng đẳng
|
1 – A |
2 – C |
3 – B |
4 – D |
5 – C |
6 – A |
7 – B |
8 – D |
9 – A |
10 – C |
Câu 10: X, Y, Z là đồng đẳng kế tiếp nên ta có:
Theo bài: chỉ có thể là
Do đó, Y là
Ta có sơ đồ:
0,1 0,3 mol
Dạng 2: Hiện tượng đồng phân
|
1 – A |
2 – A |
3 – C |
4 – B |
5 – C |
6 – C |
7 – B |
8 – A |
9 – D |
10 – A |
Xem thêm