Giáo án Hóa học 10 Chân trời sáng tạo bản word trình bày đẹp mắt, thiết kế hiện đại (chỉ từ 20k cho 1 bài Giáo án lẻ bất kì):
B1: – –
B2:
Xem thử tài liệu tại đây: Link tài liệu
|
Trường THPT …………. Tổ: ………………….. |
Họ và tên giáo viên
|
|||
|
BÀI 3: NGUYÊN TỐ HOÁ HỌC |
||||
|
Tuần: |
3 Tiết |
Ngày soạn: |
Thời gian thực hiện: |
|
I. MỤC TIÊU
1. Năng lực chung
– Tự chủ và tự học: Chủ động, tích cực tìm hiểu về nguyên tố hoá học.
– Giao tiếp và hợp tác: Sử dụng ngôn ngữ khoa học để diễn đạt khái niệm về nguyên tố hoá học, số hiệu nguyên tử và kí hiệu nguyên tử, đồng vị, nguyên tử khối; Hoạt động nhóm một cách hiệu quả theo đúng yêu cầu của giáo viên, đảm bảo các thành viên trong nhóm đều được tham gia trình bày và báo cáo.
– Giải quyết vấn đề và sáng tạo: Thảo luận với các thành viên trong nhóm nhằm giải quyết các vấn đề trong bài học, hoàn thành nhiệm vụ học tập.
2. Năng lực hóa học
– Nhận thức hoá học: Nêu được khái niệm về nguyên tố hoá học; số hiệu nguyên tử và kí hiệu nguyên tử; khái niệm đồng vị, nguyên tử khối.
– Tìm hiểu tự nhiên dưới góc độ hóa học: Tìm hiểu được ứng dụng của một số đồng vị của các nguyên tố trong tự nhiên.
– Vận dụng kiến thức, kĩ năng đã học: Tính được nguyên tử khối trung bình (theo amu) dựa vào khối lượng nguyên tử và phần trăm số nguyên tử của các đồng vị theo phổ khối lượng được cung cấp.
3. Phẩm chất
– HS có trách nhiệm tham gia tích cực trong việc hoạt động nhóm và cặp đôi phù hợp với khả năng của bản thân, hoàn thành các nội dung được giao, phát huy khả năng tư duy của HS.
– Có niềm say mê, hứng thú với việc khám phá và học tập.
– HS trung thực, nhân ái, yêu nước.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Giáo viên:
– Thiết kế phiếu học tập.
– Video, hình ảnh, các học liệu… có liên quan đến bài học.
2. Học sinh:
– Ôn tập bài cũ và chuẩn bị bài mới.
III. TIẾN TRÌNH DẠY HỌC
1. HOẠT ĐỘNG KHỞI ĐỘNG
|
a) Mục tiêu: Huy động kiến thức của học sinh tạo nhu cầu tiếp tục tìm hiểu kiến thức mới về hạt nhân nguyên tử, nguyên tố hóa học, đồng vị. b) Nội dung: GV chiếu hình ảnh, yêu cầu học sinh trả lời câu hỏi mở đầu trong SGK. c) Sản phẩm: Các câu trả lời của HS. Câu trả lời có thể đúng hoặc sai, GV không nhận xét đúng, sai mà dùng câu trả lời đó để dẫn vào bài học. d) Tổ chức thực hiện: |
|
|
HOẠT ĐỘNG CỦA GV VÀ HS |
SẢN PHẨM DỰ KIẾN |
|
Bước 1: Chuyển giao nhiệm vụ học tập: – GV chiếu hình ảnh, yêu cầu học sinh thảo luận và trả lời câu hỏi:
Kim cương và than chì có vẻ ngoài khác nhau. Tuy nhiên, chúng đều được tạo thành từ cùng một nguyên tố hóa học là nguyên tố carbon (C). Nguyên tố hóa học là gì? Một nguyên tử của nguyên tố hóa học có những đặc trưng cơ bản nào? Bước 2: Thực hiện nhiệm vụ: HS hoạt động cá nhân ghi câu trả lời. GV theo dõi hỗ trợ. Bước 3: Báo cáo kết quả và thảo luận: GV yêu cầu đại diện 1 HS trình bày. Bước 4: Kết luận và nhận định: GV không nhận xét đúng, sai mà dùng câu trả lời đó để dẫn vào bài học. |
– Nguyên tố hóa học là tập hợp những nguyên tử có cùng điện tích hạt nhân. – Số đơn vị điện tích hạt nhân nguyên tử (còn gọi là số hiệu nguyên tử) của một nguyên tố hóa học và số khối được xem là những đặc trưng cơ bản của nguyên tử.
|
2. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
|
Hoạt động 1: Hạt nhân nguyên tử a) Mục tiêu: Xác định được điện tích hạt nhân, số khối của nguyên tử. b) Nội dung: HS nghiên cứu SGK, trả lời câu hỏi của GV. c) Sản phẩm: Các câu trả lời của HS. d) Tổ chức thực hiện: |
|
|
HOẠT ĐỘNG CỦA GV VÀ HS |
SẢN PHẨM DỰ KIẾN |
|
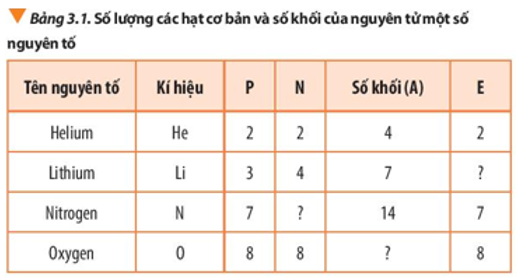
Bước 1: Chuyển giao nhiệm vụ học tập: Nhiệm vụ 1: – GV yêu cầu HS nghiên cứu SGK và thảo luận theo bàn: Quan sát hình 3.1 trang 20 SGK, cho biết nguyên tử nitrogen có bao nhiêu proton, neutron và electron. Điện tích hạt nhân và số khối của nguyên tử nitrogen là bao nhiêu? Nhiệm vụ 2: – GV yêu cầu HS nghiên cứu SGK và thảo luận theo bàn: Hoàn thiện nội dung trong bảng 3.1:
Bước 2: Thực hiện nhiệm vụ: HS hoạt động theo bàn lần lượt thực hiện các nhiệm vụ GV yêu cầu. Các nhóm thảo luận và ghi câu trả lời. GV theo dõi và hỗ trợ cho nhóm HS. Bước 3: Báo cáo kết quả và thảo luận: GV yêu cầu đại diện 2 nhóm bất kì trình bày kết quả thảo luận của nhóm (mỗi nhóm trình bày kết quả 1 nhiệm vụ), các HS khác chú ý theo dõi.
Bước 4: Kết luận và nhận định: HS nhận xét sản phẩm của nhóm khác. GV nhận xét, đưa ra kết luận, chốt kiến thức. |
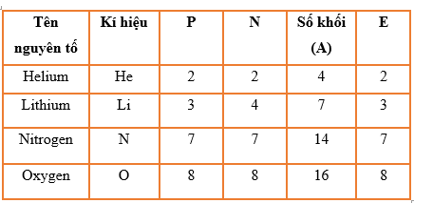
Kết quả nhiệm vụ 1: Dựa vào hình 3.1 ta thấy: Nguyên tử nitrogen có 7 proton, 7 neutron và 7 electron. Nguyên tử nitrogen có số đơn vị điện tích hạt nhân Z = số proton = 7. Điện tích hạt nhân của nguyên tử nitrogen bằng +Z = +7. Kết quả nhiệm vụ 2:
|
|
Kiến thức trọng tâm – Số đơn vị điện tích hạt nhân (Z) = số proton (P) = số electron (E). – Điện tích hạt nhân = +Z. – Số khối (A) = số proton (P) + số neutron (N). |
|
|
Hoạt động 2: Nguyên tố hóa học a) Mục tiêu: – Biết được định nghĩa về nguyên tố hóa học, số hiệu nguyên tử. b) Nội dung: HS thảo luận nhóm hoàn thiện phiếu học tập số 1 c) Sản phẩm: Lời giải phiếu học tập số 1. d) Tổ chức thực hiện: |
|
|
Hoạt động của GV và HS |
Sản phẩm dự kiến |
|
Bước 1: Chuyển giao nhiệm vụ học tập: – Chia lớp làm 4 nhóm. – Yêu cầu HS nghiên cứu tài liệu SGK trang 21 – 22, thảo luận nhóm và hoàn thành phiếu học tập số 1: PHIẾU HỌC TẬP SỐ 1 1. Nguyên tố hóa học là gì? 2. Các nguyên tử thuộc cùng một nguyên tố hóa học có tính chất hóa học giống hay khác nhau? 3. Cho các nguyên tử sau: B (Z = 8; A = 16); D (Z = 7; A = 15); E (Z = 8; A = 18). Trong các nguyên tử trên, các nguyên tử nào thuộc cùng một nguyên tố hoá học? – HS nhận nhiệp vụ. Bước 2: Thực hiện nhiệm vụ: HS tham gia hoạt động nhóm, thảo luận nhóm và đưa ra câu trả lời ở phiếu số 1. Ghi chép lại những gì học được, những ý hay của bạn. GV theo dõi và hỗ trợ cho nhóm HS. Bước 3: Báo cáo kết quả và thảo luận: – GV gọi đại diện 1 nhóm trả lời câu hỏi trong phiếu học tập. Bước 4: Kết luận và nhận định: – Học sinh nhận xét, bổ sung, đánh giá sản phẩm của nhóm khác. – Giáo viên nhận xét, đánh giá, đưa ra kết luận, chốt kiến thức. Thông tin thêm: Cho đến 2016, con người đã biết 118 nguyên tố hóa học, trong đó có 94 nguyên tố có trong tự nhiên và khoảng 24 nguyên tố nhân tạo. |
2. Nguyên tố hóa học
PHIẾU HỌC TẬP SỐ 1 1. Nguyên tố hóa học là tập hợp những nguyên tử có cùng điện tích hạt nhân. 2. Các nguyên tử của cùng 1 nguyên tố có tính chất hoá học giống nhau. 3. B và E thuộc cùng 1 nguyên tố hoá học vì có cùng số đơn vị điện tích hạt nhân. |
|
Kiến thức trọng tâm – Số đơn vị điện tích hạt nhân nguyên tử của một nguyên tố được gọi là số hiệu nguyên tử (Z) của nguyên tố đó. – Mỗi nguyên tố hoá học có một số hiệu nguyên tử. – Nguyên tố hoá học là tập hợp những nguyên tử có cùng điện tích hạt nhân. |
|
…………………………………………
…………………………………………
…………………………………………
Tài liệu có 16 trang, trên đây trình bày tóm tắt 6 trang của Giáo án Hóa hoc 10 Chân trời sáng tạo Bài 3: Nguyên tố hóa học.
Xem thêm các bài giáo án Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Giáo án Bài 2: Thành phần của nguyên tử
Giáo án Bài 3: Nguyên tố hoá học
Giáo án Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
Giáo án Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
Giáo án Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kỳ và nhóm
Để mua Giáo án Hóa học 10 Chân trời sáng tạo năm 2023 mới nhất, mời Thầy/Cô liên hệ https://tailieugiaovien.com.vn/