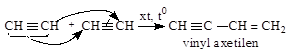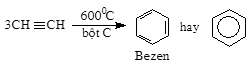Tiết 48 – Bài 32: ANKIN
I/ Mục TIÊU BÀI HỌC
1. Kiến thức
Biết được:
– Định nghĩa, công thức chung, đặc điểm cấu tạo, đồng phân, danh pháp, tính chất vật lí (quy luật biến đổi về trạng thái, nhiệt độ nóng chảy, nhiệt độ sôi, khối lượng riêng, tính tan) của ankin.
– Tính chất hoá học của ankin: Phản ứng cộng H2, Br2, HX ; Phản ứng thế nguyên tử H linh động của ank-1-in ; phản ứng oxi hoá).
– Điều chế axetilen trong phòng thí nghiệm và trong công nghiệp.
2. Kĩ năng
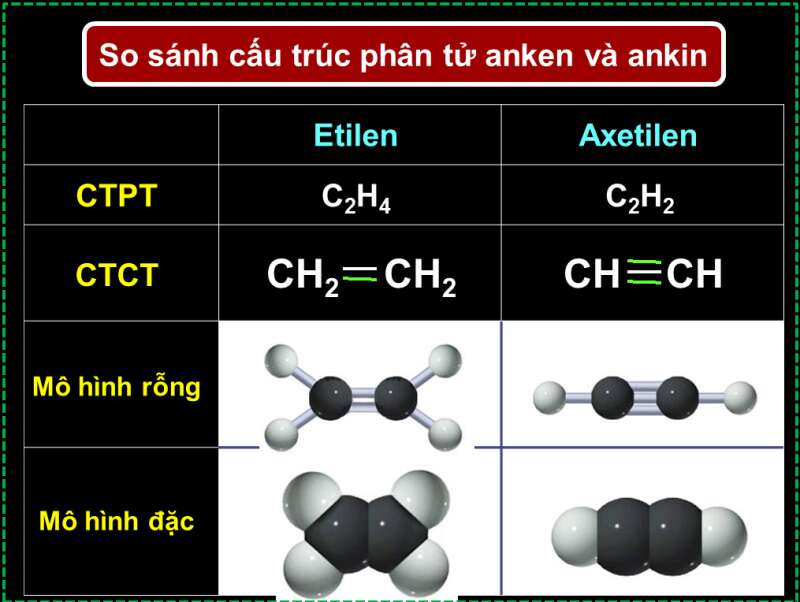
– Quan sát được thí nghiệm, mô hình phân tử, rút ra nhận xét về cấu tạo và tính chất của ankin.
– Viết được công thức cấu tạo của một số ankin cụ thể.
– Dự đoán được tính chất hoá học, kiểm tra và kết luận.
– Viết được các phương trình hoá học biểu diễn tính chất hoá học của axetilen.
– Phân biệt ank-1-in với anken và các ankin khác bằng phương pháp hoá học.
– Tính thành phần phần trăm về thể tích khí trong hỗn hợp.
II/ TRỌNG TÂM
– Dãy đồng đẳng, đặc điểm cấu trúc phân tử, đồng phân và cách gọi tên theo danh pháp thông thường, danh pháp hệ thống của ankin.
– Tính chất hoá học của ankin.
– Phương pháp điều chế axetilen trong phòng thí nghiệm, trong công nghiệp.
III/ Chuẩn bị
Hoá chất, dụng cụ thí nghiệm: CaC2, nước cất, dung dịch AgNO3, dung dịch NH3, dung dịch brom, dung dịch KMnO4 ; 1 ống nghiệm 2 nhánh, 3 kẹp ống nghiệm, 3 ống nghiệm, 1 giá đở, ống dẫn khí, giá ống nghiệm…
IV/ Phương pháp
Trực quan, đàm thoại, phát vấn, nêu vấn đề…
V/ Các bước thực hiện
1/ Ổn định lớp: Kiểm tra sĩ số, nắm tình hình lớp.
2/ Học bài mới: HOẠT ĐỘNG 1 (5 phút)
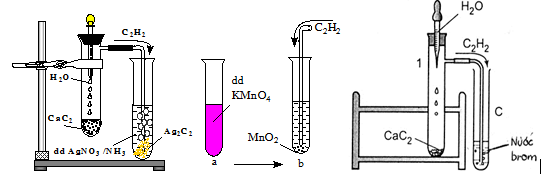
GV làm thí nghiệm điều chế khí axetilen và sục khí đó vào các dung dịch AgNO3/NH3, dung dịch brom, dung dịch KMnO4 và đốt cháy. Yêu cầu HS rút ra hiện tượng để tìm hiểu về TCHH của Ankin.
|
HOẠT ĐỘNG CỦA GV |
HOẠT ĐỘNG CỦA HS |
NỘI DUNG |
|||
|
HOẠT ĐỘNG 2 (5 phút) I. ĐỒNG ĐẲNG, ĐỒNG PHÂN, DANH PHÁP |
|||||
|
– GV lấy ví dụ ankin đơn giản nhất là: CH≡CH (axetilen). Yêu cầu HS ghi CTPT một số đồng đẳng của axetilen và CTTQ của ankin. – GV nêu cấu tạo hóa học một số ankin. Yêu cầu HS rút ra khái niệm ankin.
|
– C3H4 ; C4H6 … CnH2n – 2
– Cấu tạo: mạch hở, chứa 1 liên kết ba. => Ankin là hiđrocacbon không no, mạch hở có 1 liên kết ba trong phân tử và CTTQ: CnH2n – 2, n ≥ 2. |
1. Dãy đồng đẳng ankin CTPT CTCT C2H2 (CH≡CH) Axetilen C3H4 (CH≡C-CH3) C4H6 (CH≡C-CH2-CH3) … CnH2n – 2 => Gọi là dãy đồng đẳng ankin. Nhận xét: Ankin là hiđrocacbon không no, mạch hở có 1 liên kết ba trong phân tử và CTTQ: CnH2n – 2, n ≥ 2. |
|||
|
– GV hướng dẫn cách viết đồng phân ankin có CTPT C5H8 và phân loại đồng phân ankin. Các đồng phân ankin không có đồng phân hình học như anken.
– Yêu cầu HS dựa vào kiến thức đồng phân, viết CTCT của các ankin có CTPT C4H6. Từ đó rút ra nhận xét. |
– HS áp dụng viết CTCT của các ankin có công thức phân tử: C4H6. Phân loại các đồng phân vừa viết được. |
2. Đồng phân * Ankin từ C4 trở đi có đồng phân vị trí liên kết ba và đồng phân mạch cacbon. * Ví dụ: |
|||
|
C5H8
BT1: C4H6
|
CH≡C–CH2–CH2 –CH3, CH3–C≡C–CH2 – CH3, CH≡C–CH2–CH3 và CH3 – C ≡C – CH3 |
||||
|
HOẠT ĐỘNG 3 (5 phút) |
|||||
|
– GV đưa các CTCT ankin và gọi tên thông thường tương ứng. Từ đó yêu cầu HS rút ra cách gọi tên thông thường.
– GV đưa ra một CTCT, đưa tên gọi của nó và cho HS biết quy tắc gọi tên thay thế ankin tương tự như anken, nhưng dùng vần in để chỉ liên kết ba. GV giới thiệu về ank-1-in.
– GV đưa CTCT một ankin khác yêu cầu HS áp dụng gọi tên.
|
– HS nắm kiến thức và áp dụng rút ra qui tắc tên gọi thường.
– HS nắm kiến thức và áp dụng gọi tên. |
3. Danh pháp 3.a. Tên thông thường Ví dụ: CH≡C–CH2–CH2–CH3 propylaxetilen CH3–C≡C–CH3 đimetylaxetilen CH3–C≡C–CH2 – CH3 Etylmetylaxetilen Qui tắc: Tên gốc ankyl (nếu nhiều gốc khác nhau thì đọc theo thứ tự A, B, C) liên kết với nguyên tử C của liên kết ba + axetilen. 3.b. Tên thay thế (Tên IUPAC) Ví dụ: 3-metylbut-1-in Qui tắc: Tiến hành tương tự như đối với anken, nhưng dùng vần in để chỉ liên kết ba. » Các ankin có liên kết ba ở đầu mạch (dạng R-C≡CH) gọi chung là các ank -1-in.
BT2: CH3–C≡ C–CH–CH3 CH3 4-metylpent-2-in |
|||
|
HOẠT ĐỘNG 4 (2 phút) II. TÍNH CHẤT VẬT LÍ |
|||||
|
– GV hướng dẫn HS nghiên cứu SGK và trả lời câu hỏi liên quan đến tính chất vật lí: trạng thái; qui luất biến đổi về nhiệt độ nóng chảy, nhiệt độ sôi, khối lượng riêng; tính tan. – GV nói thêm: Riêng C2H2 tan khá dễ trong axeton. |
– HS nghiên cứu SGK (theo bảng 6.2 và tính chất vật lí nêu trong trang 140 SGK) trả lời câu hỏi của GV. |
(Như các hiđrocacbon khác) – Trạng thái – Nhiệt độ nóng chảy, nhiệt độ sôi – Khối lượng riêng – Tính tan (SGK) |
|||
|
HOẠT ĐỘNG 5 (10 phút) III. TÍNH CHẤT HOÁ HỌC |
|||||
|
– GV nêu vấn đề: Từ đặc điểm cấu tạo của anken và ankin hãy dự đoán về tính chất hoá học của ankin? – GV thông báo các phản ứng của ankin.
– GV hướng dẫn HS viết PTHH của phản ứng cộng ankin với các tác nhân H2, X2, HX. Lưu ý HS: phản ứng xảy ra theo hai giai đoạn liên tiếp và cũng tuân theo qui tắc Mac-côp-nhi-côp. – Phân tích kĩ phản ứng của ankin với HX về điều kiện phản ứng, sự hình thành sản phẩm, đây là những phản ứng thể hiện ứng dụng của ankin.
|
– HS phát biểu: phản ứng cộng ankin với các tác nhân H2, X2, HX
– HS nắm kiến thức.
– HS viết PTHH. |
1. Phản ứng cộng 1.a. Cộng H2 với xúc tác Ni, t0 + Cộng liên tiếp theo hai giai đoạn: CHCH + H2 CH2=CH2 CH2=CH2+ H2CH3-CH3 Với xúc tác Pd/PbCO3 hoặc Pd/ BaSO4 phản ứng dừng lại tạo anken. CHCH+H2 CH2=CH2 Ứng dụng: phản ứng dùng để điều chế anken từ ankin. 1.b. Cộng brom, clo + Cộng theo hai giai đoạn: CHCH + Br2 ” CHBr = CHBr 1,2 – đibrometen CHBr=CHBr + Br2” CHBr2-CHBr2 1,1,2,2-tetrabrometan 1.c. Cộng HX (X là OH, Cl, Br, CH3COO…) phản ứng tuân theo qui tắc Mac-côp-nhi-côp. + Cộng liên tiếp theo hai giai đoạn: CHCH + HClCH2=CHCl vinylclorua CH2=CHCl+ HClCH3-CHCl2 1,1- đicloetan Nếu (xt) thích hợp phản ứng dừng lại ở sản phẩm chứa nối đôi (dẫn xuất monoclo của anken). CHCH + HClCH2=CHCl vinylclorua |
|||
|
Quan trọng là: Phản ứng cộng H2O theo tỉ lệ: 1 : 1
không bền anđehit axetic |
|||||
|
– GV giới thiệu về phản ứng đime và trime hóa, thông báo: các phản ứng này có ứng dụng trong thực tiễn. Tổng hợp cao su và điều chế benzen. |
1.d. Phản ứng đime và trime hoá: |
||||
|
+ Phản ứng đime hoá: + Phản ứng trime hoá:
|
|||||
|
HOẠT ĐỘNG 6 (5 phút) |
|||||
|
– GV cho HS viết PTHH dạng tổng quát và rút ra nhận xét so sánh số mol CO2 và H2O.
– GV phát biểu về phản ứng oxi hóa không hoàn toàn. |
– HS viết PTHH của phản ứng tổng quát và nhận xét.
– HS nắm kiến thức. |
2. Phản ứng oxi hoá
2.a. Phản ứng oxi hoá hoàn toàn. CnH2n -2 + (3n-1)/2 O2 nCO2 + (n-1)H2O Nhận xét: nCO2 > nH2O nCO2 – nH2O = nankin 2.b. Phản ứng oxi hoá không hoàn toàn. Các ankin dễ làm mất màu dung dịch brom và thuốc tím như các anken. |
|||
|
HOẠT ĐỘNG 7 (5 phút) |
|||||
|
– Yêu cầu HS viết PTHH xảy ra và GV đưa PTHH tổng quát.
– GV và HS rút ra nhận xét.
– GV đưa ví dụ yêu cầu HS hoạt động nhóm viết PTHH xảy ra. |
– HS viết PTHH.
– HS nhận xét.
– HS hoạt động nhóm viết PTHH.
|
3. Phản ứng thế bằng ion kim loại CHCH+2AgNO3+2NH3 Ag – C C – Ag + 2NH4NO3 bạc axetilua ( Ag2C2 màu vàng) Nhận xét: + Nguyên tử H liên kết với nguyên tử C nối ba linh động hơn các nguyên tử H khác nên dễ bị thay thế bằng ion kim loại. + Phản ứng thế của ank-1-in với dung dịch AgNO3/ NH3 giúp phân biệt ank-1-in với các ankin khác. BT3: CH≡C-CH3 + HCl CH≡C-CH3 + H2O CH≡C-CH3 + AgNO3+NH3 |
|||
|
HOẠT ĐỘNG 8 (5 phút) IV. ĐIỀU CHẾ |
|||||
|
– GV hướng dẫn HS viết PTHH của phản ứng điều chế axetilen trong PTN và trong CN. |
– HS viết PTHH của phản ứng điều chế axetilen trong PTN và trong CN. |
1. Trong PTN. CaC2+2H2O C2H2 + Ca(OH)2 CaC2: đất đèn (canxi cacbua). 2. Trong CN. Từ metan. 2CH4 C2H2 + 3H2 |
|||
|
V. ỨNG DỤNG |
|||||
|
– GV cho HS tìm hiểu SGK rút ra những ứng dụng của axetilen. |
– HS tìm hiểu SGK rút ra những ứng dụng của axetilen. |
+ Làm nhiên liệu: hàn cắt, đèn xì… + Làm nguyên liệu sản xuất hoá hữu cơ: sản xuất PVC, tơ sợi tổng hợp, axit hữu cơ, este… |
|||
|
HOẠT ĐỘNG 9 (2 phút) CỦNG CỐ BÀI HỌC |
|||||
|
GV nhắc lại những kiến thức cần củng cố: + Phản ứng cộng của ankin, phản ứng thế ion kim loại, kĩ năng viết PTHH trọng tâm. + Áp dụng kiến thức vừa học giải quyết bài tập củng cố: Bài 1:
Bài 2: |
|||||
HOẠT ĐỘNG 10 (1 phút)
DẶN DÒ
+ Chuẩn bị bài Luyện tập Ankin.
+ Bài tập về nhà: 1, 2, 3, 4, 5 trang 145 SGK.
PHIẾU HỌC TẬP
BT1: Viết các đồng phân ankin có CTPT là C4H6 ?
BT2: Gọi tên thường và tên thay thế ankin có CTCT sau:
CH3–C≡ C–CH–CH3
│
CH3
BT3: Viết các PTHH xảy ra và ghi rỏ điều kiện nếu có của các phản ứng sau?
CH≡C-CH3 + HCl
CH≡C-CH3 + H2O
CH≡C-CH3 + AgNO3+NH3
BÀI TẬP CỦNG CỐ
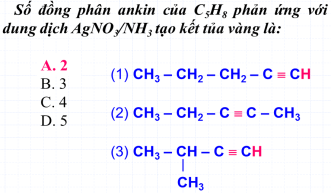
BÀI 1: Số đồng phân ankin của C5H8 phản ứng với dung dịch AgNO3/NH3 tạo kết tủa vàng là:
A. 2 B. 3 C. 4 D. 5
BÀI 2: Bằng phương pháp hóa học, hãy phân biết 3 bình mất nhãn chứa mổi khí không màu sau: etan, etilen, axetilen.
Và các bài tập SGK và bài tập thêm do GV cung cấp!!!
Xem thêm